Czym są wyroby medyczne?
Wyroby medyczne to instrumenty, aparatura, maszyny, implanty lub oprogramowanie przeznaczone do celów medycznych, takich jak diagnozowanie, zapobieganie, monitorowanie lub leczenie chorób i urazów. Produkty te obejmują zarówno proste szpatułki, jak i złożone programowalne rozruszniki serca i sztuczne narządy.
Światowa Organizacja Zdrowia szacuje, że na całym świecie istnieje około 2 miliony różnych rodzajów wyrobów medycznych, podzielonych na ponad 7000 ogólnych grup wyrobów. Ten rozległy ekosystem obejmuje wszystko, od bandaży i stetoskopów po sztuczne serca i zrobotyzowane systemy chirurgiczne.
Definiowanie wyrobów medycznych
Definicja regulacyjna różni się w zależności od jurysdykcji, ale podstawowa koncepcja pozostaje spójna. W Stanach Zjednoczonych sekcja 201 (h) federalnej ustawy o żywności, lekach i kosmetykach definiuje wyrób medyczny jako „instrument, aparat, narzędzie, maszynę, urządzenie, implant, odczynnik in vitro lub inny podobny artykuł” przeznaczony do celów medycznych, który nie osiąga swojego podstawowego działania w organizmie za pomocą środków chemicznych.
To rozróżnienie oddziela wyroby medyczne od leków. Podczas gdy leki działają poprzez działanie chemiczne lub metaboliczne, urządzenia działają za pomocą środków fizycznych, mechanicznych lub elektronicznych. Ciśnieniomierz mierzy ciśnienie fizyczne,-aparat rentgenowski wykorzystuje promieniowanie, a rozrusznik serca dostarcza impulsy elektryczne-żadne z nich nie opiera się na reakcjach chemicznych, aby osiągnąć swój główny cel.
Nowoczesne definicje zostały poszerzone i obejmują oprogramowanie jako wyrób medyczny (SaMD), uznając, że samodzielne aplikacje spełniające funkcje medyczne kwalifikują się jako urządzenia nawet bez fizycznych komponentów sprzętowych. Aplikacje mobilne analizujące dane pacjenta, algorytmy diagnostyczne i systemy wspomagania decyzji klinicznych podlegają obecnie przepisom dotyczącym wyrobów medycznych.
Systemy klasyfikacji
Agencje regulacyjne na całym świecie klasyfikują wyroby medyczne na podstawie poziomów ryzyka, chociaż konkretne systemy różnią się w zależności od regionu.
Klasyfikacja Stanów Zjednoczonych
FDA dzieli urządzenia na trzy klasy w oparciu o potencjalne ryzyko dla pacjenta i wymaganą kontrolę regulacyjną:
Urządzenia klasy Ireprezentują najniższą kategorię ryzyka. Produkty te powodują minimalne potencjalne szkody i obejmują takie elementy, jak bandaże elastyczne, rękawiczki badawcze i ręczne narzędzia chirurgiczne. Około 47% wyrobów medycznych należy do klasy I. Większość z nich jest zwolniona z wymogów dotyczących powiadamiania przed wprowadzeniem do obrotu, chociaż producenci muszą nadal przestrzegać ogólnych kontroli, w tym rejestracji zakładu, wykazu wyrobów i dobrych praktyk produkcyjnych.
Urządzenia klasy IIniosą ze sobą umiarkowane ryzyko i wymagają większego nadzoru niż produkty klasy I. Kategoria ta obejmuje wózki inwalidzkie z napędem elektrycznym, pompy infuzyjne, obłożenia chirurgiczne i zestawy do przetaczania krwi. Urządzenia klasy II zazwyczaj wymagają powiadomienia przed wprowadzeniem na rynek zgodnie z normą 510(k), wykazującego znaczną równoważność z urządzeniem sprzedawanym legalnie. Produkty te stanowią około 43% wszystkich wyrobów medycznych.
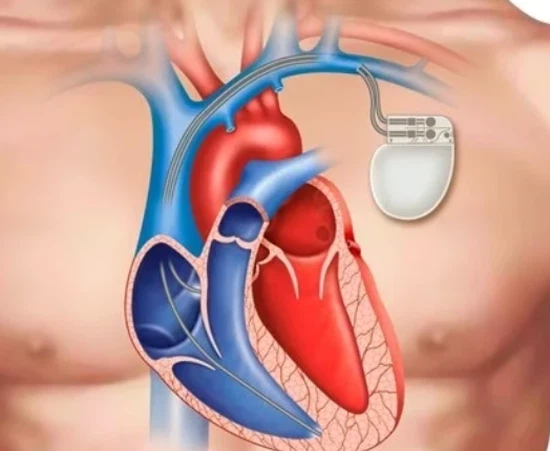
Urządzenia klasy IIIstwarzają największe ryzyko-podtrzymują lub podtrzymują życie, są wszczepione lub mogą powodować nadmierne ryzyko choroby lub urazu. Przykładami mogą być rozruszniki serca, zastawki serca i wszczepialne defibrylatory. Tylko 10% wyrobów medycznych należy do klasy III, ale przechodzą one najbardziej rygorystyczny proces zatwierdzania przed wprowadzeniem na rynek, wymagający danych klinicznych potwierdzających bezpieczeństwo i skuteczność.
Klasyfikacja Unii Europejskiej
System UE wykorzystuje cztery kategorie ryzyka zgodnie z rozporządzeniem w sprawie wyrobów medycznych (UE) 2017/745:
Klasa I obejmuje nieinwazyjne-wyroby niskiego ryzyka-, takie jak bandaże i pomoce do chodzenia. Klasa IIa obejmuje wyroby-średniego ryzyka, takie jak soczewki kontaktowe i aparaty słuchowe. Klasa IIb obejmuje urządzenia-wyższego ryzyka, w tym wentylatory i lasery chirurgiczne. Klasa III reprezentuje najwyższą kategorię ryzyka dla urządzeń-podtrzymujących życie lub wszczepianych.
Klasyfikacja określa wymagania dotyczące oceny zgodności. Urządzenia klasy I (z wyjątkiem urządzeń sterylnych lub pomiarowych) mogą być-samodzielnie certyfikowane przez producentów, natomiast wyższe klasy wymagają oceny przez jednostki notyfikowane-niezależne organizacje upoważnione do oceny zgodności wyrobów.
Rodzaje wyrobów medycznych
Urządzenia medyczne pełnią różnorodne funkcje opieki zdrowotnej w wielu kategoriach.
Sprzęt diagnostyczny
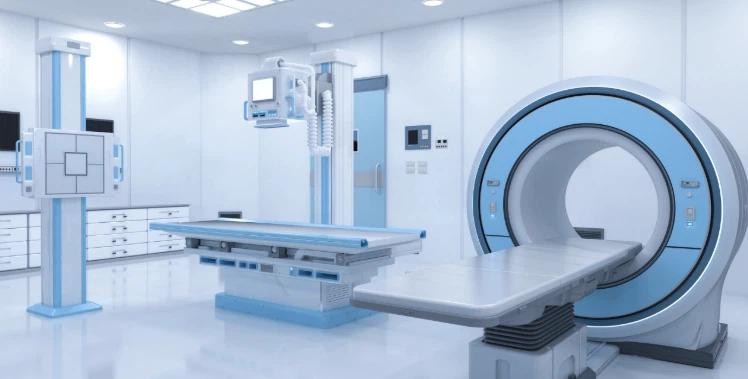
Urządzenia diagnostyczne pomagają pracownikom służby zdrowia ocenić stan zdrowia pacjentów. Technologie obrazowania, takie jak aparaty rentgenowskie, skanery MRI, tomograf komputerowy i systemy ultradźwiękowe, wizualizują struktury wewnętrzne i wykrywają nieprawidłowości. Sprzęt laboratoryjny, w tym mikroskopy, wirówki i spektrofotometry, analizuje krew, tkanki i inne próbki biologiczne. Przyłóżkowe urządzenia diagnostyczne, takie jak glukometry, testy ciążowe i szybkie testy na obecność wirusa COVID-19, umożliwiają przeprowadzanie badań poza tradycyjnymi warunkami laboratoryjnymi.
Urządzenia terapeutyczne i lecznicze
Urządzenia te zapewniają leczenie lub interwencje terapeutyczne. Pompy infuzyjne podają dożylnie kontrolowane ilości leków, płynów lub składników odżywczych. Narzędzia chirurgiczne, w tym skalpele, kleszcze, retraktory i zszywacze chirurgiczne, umożliwiają precyzyjne zabiegi. Sprzęt do radioterapii leczy pacjentów chorych na raka celowanymi dawkami promieniowania. Urządzenia wszczepialne, takie jak implanty ślimakowe, przywracają słuch, a sztuczne stawy zastępują uszkodzone biodra, kolana i ramiona.
Sprzęt monitorujący
Urządzenia monitorujące śledzą parametry życiowe i fizjologiczne pacjenta. Ciśnieniomierze, pulsoksymetry, kardiomonitory i ciągłe monitory poziomu glukozy dostarczają-danych zdrowotnych w czasie rzeczywistym. Urządzenia do noszenia, w tym monitory kondycji i inteligentne zegarki, coraz częściej zawierają czujniki-klasy medycznej umożliwiające ciągłe monitorowanie stanu zdrowia. Systemy zdalnego monitorowania pacjentów przesyłają dane ze ustawień domowych do podmiotów świadczących opiekę zdrowotną, umożliwiając wirtualną opiekę.
Sprzęt do podtrzymywania życia
Urządzenia do intensywnej terapii podtrzymują ważne funkcje organizmu. Wentylatory mechaniczne wspomagają lub zastępują funkcję oddychania u pacjentów niezdolnych do samodzielnego oddychania. Podczas operacji płuco-serce i płuca tymczasowo przejmują funkcje serca i układu oddechowego. Maszyny do dializy filtrują krew dla pacjentów z niewydolnością nerek. Urządzenia do pozaustrojowego natleniania membranowego (ECMO) zapewniają wsparcie serca i układu oddechowego krytycznie chorym pacjentom.
Urządzenia wspomagające
Technologie wspomagające pomagają osobom niepełnosprawnym zachować niezależność. Urządzenia ułatwiające poruszanie się, w tym wózki inwalidzkie, chodziki, laski i aparaty ortodontyczne, wspomagają ruch. Protezy kończyn zastępują brakujące części ciała. Aparaty słuchowe wzmacniają dźwięk u osób z ubytkiem słuchu. Pomoce wzrokowe, w tym lupy i czytniki ekranu, pomagają osobom niedowidzącym.
Technologie produkcyjne
Produkcja wyrobów medycznych wymaga precyzyjnych technik produkcji, które spełniają rygorystyczne normy jakości i bezpieczeństwa.
Tradycyjne metody obróbki, takie jak frezowanie i toczenie CNC, tworzą komponenty poprzez usuwanie materiału. Te procesy odejmowania sprawdzają się dobrze w przypadku prostszych geometrii, ale stają się kosztowne i-czasochłonne w przypadku skomplikowanych kształtów.
Formowanie wtryskowe metali(MIM) okazała się cenną techniką wytwarzania wyrobów medycznych. Proces ten łączy proszek metalowy ze spoiwem w celu wytworzenia surowca, który jest formowany wtryskowo w złożone kształty, a następnie spiekany w celu wytworzenia gęstych elementów metalowych. MIM specjalizuje się w tworzeniu skomplikowanych narzędzi chirurgicznych, zamków ortodontycznych i elementów urządzeń wszczepialnych o wąskich tolerancjach i doskonałym wykończeniu powierzchni. Technologia ta przynosi szczególne korzyści w produkcji małych, skomplikowanych części w dużych seriach, oferując przewagę kosztową w porównaniu z tradycyjną obróbką skrawaniem, jednocześnie umożliwiając uzyskanie geometrii projektowych trudnych lub niemożliwych do osiągnięcia w inny sposób.
Produkcja przyrostowa (druk 3D) polega na tworzeniu komponentów warstwa po warstwie, umożliwiając-dostosowanie do potrzeb pacjenta. Dzięki tej technologii powstają spersonalizowane implanty, prowadnice chirurgiczne i protezy dostosowane do indywidualnej anatomii.
Aktualne trendy i innowacje
Branża wyrobów medycznych kontynuuje szybką ewolucję napędzaną postępem technologicznym i zmieniającymi się potrzebami opieki zdrowotnej.
Integracja sztucznej inteligencji
Sztuczna inteligencja i uczenie maszynowe zmieniają możliwości urządzeń. Systemy obrazowania diagnostycznego wykorzystują obecnie algorytmy sztucznej inteligencji, które wykrywają nieprawidłowości, czasami z dokładnością przewyższającą radiologów. Urządzenia ubieralne wykorzystują uczenie maszynowe do przewidywania zdarzeń zdrowotnych, zanim pojawią się objawy. Roboty chirurgiczne wykorzystują sztuczną inteligencję w celu zwiększenia precyzji i autonomicznego wykonywania zadań.
FDA zatwierdziła wiele urządzeń-obsługujących sztuczną inteligencję, obejmujących cyfrowe rozwiązania terapeutyczne wykorzystujące algorytmy sztucznej inteligencji do leczenia takich schorzeń, jak bezsenność, zaburzenia związane z używaniem substancji psychoaktywnych i przewlekły ból, za pomocą interwencji opartych na oprogramowaniu-.
Połączone urządzenia medyczne
Internet rzeczy medycznych (IoMT) tworzy sieci połączonych urządzeń, które przesyłają i analizują dane dotyczące zdrowia w czasie rzeczywistym. Pompy insulinowe komunikują się z ciągłymi monitorami poziomu glukozy, aby automatycznie dostosowywać podaż na podstawie poziomu cukru we krwi. Systemy szpitalne wykorzystują podłączone urządzenia do zdalnego monitorowania pacjentów i powiadamiania personelu o istotnych zmianach.
Począwszy od 2024 r., połączone urządzenia generowały ponad 2,5 miliarda punktów danych rocznie, umożliwiając wgląd w stan zdrowia populacji i analizy predykcyjne, które usprawniają świadczenie opieki.
Miniaturyzacja i przenośność
Miniaturyzacja urządzeń umożliwia nowe zastosowania. Połknięte czujniki wielkości pigułek monitorują stan wewnętrzny organizmu. Instrumenty mikro-chirurgiczne umożliwiają wykonywanie zabiegów za pomocą małych nacięć. Przenośne urządzenia diagnostyczne umożliwiają szpitalne-testowanie jakości w odległych lokalizacjach i w domu.
Na rynku w 2024 r. odnotowano znaczny wzrost-domowych urządzeń diagnostycznych, wykraczający poza badania na obecność wirusa Covid-19 i obejmujące zakażenia dróg moczowych, niedobory witamin i poziom hormonów.
Spersonalizowane urządzenia medyczne
Niestandardowe urządzenia dostosowane do indywidualnych potrzeb pacjentów stwarzają rosnące możliwości.. 3D-drukowane implanty precyzyjnie dopasowują się do anatomii pacjenta. Urządzenia do podawania leków dostosowują dawkowanie na podstawie danych-biomarkerów w czasie rzeczywistym. Urządzenia do badań genetycznych pozwalają na kształtowanie spersonalizowanych strategii leczenia.

Wymagania regulacyjne
Regulacja wyrobów medycznych zapewnia bezpieczeństwo pacjenta, jednocześnie umożliwiając wprowadzanie innowacji.
Wymagania przed wprowadzeniem na rynek
Producenci muszą wykazać bezpieczeństwo i skuteczność urządzenia przed wprowadzeniem go na rynek. Konkretna ścieżka zależy od klasyfikacji i poziomu ryzyka. Urządzenia klasy I często kwalifikują się do zwolnień. Urządzenia klasy II zazwyczaj wymagają powiadomienia przed wprowadzeniem na rynek zgodnie z przepisami 510(k). Wyroby klasy III wymagają zatwierdzenia przed wprowadzeniem na rynek wraz z obszernymi danymi klinicznymi.
Proces obejmuje dokumentowanie zamierzonego zastosowania, specyfikacji projektowych, procesów produkcyjnych, testów wydajności, weryfikacji biokompatybilności oraz dowodów klinicznych potwierdzających twierdzenia o bezpieczeństwie i skuteczności.
Systemy Zarządzania Jakością
Producenci muszą ustanowić systemy zarządzania jakością zapewniające stałą jakość wyrobów. Przepisy FDA wymagają zgodności z przepisami dotyczącymi systemu jakości 21 CFR część 820. Międzynarodowi producenci przestrzegają normy ISO 13485, uznanej na całym świecie normy zarządzania jakością wyrobów medycznych.
Systemy te obejmują kontrolę projektu, procesy produkcyjne, zarządzanie dostawcami, działania korygujące i zapobiegawcze oraz procedury rozpatrywania reklamacji.
Post-Nadzór rynku
Nadzór regulacyjny trwa po zatwierdzeniu przez rynek. Producenci muszą zgłaszać zdarzenia niepożądane, przeprowadzać-badania po nadzorze rynku i śledzić-wyroby wysokiego ryzyka. Przepisy FDA dotyczące zgłaszania wyrobów medycznych wymagają szybkiego zgłaszania zgonów, poważnych obrażeń lub awarii urządzeń.
Dane po-rynku informują o potencjalnym wycofaniu produktu, komunikatach dotyczących bezpieczeństwa i aktualizacjach etykiet chroniących bezpieczeństwo pacjentów przez cały cykl życia urządzenia.
Dynamika rynku
Globalny rynek wyrobów medycznych wykazuje silny wzrost napędzany trendami demograficznymi i innowacjami technologicznymi.
Amerykański rynek wyrobów medycznych osiągnął w 2024 r. wartość 188,68 miliarda dolarów, a prognozy mają wzrosnąć do 314,96 miliarda dolarów do 2032 roku, przy złożonej rocznej stopie wzrostu wynoszącej 6,8%. Prognozy rynku światowego przewidują przychody w wysokości 595 miliardów dolarów w 2024 roku.
Ekspansję rynku napędza kilka czynników. Starzejące się populacje w krajach rozwiniętych zwiększają zapotrzebowanie na urządzenia terapeutyczne i monitorujące. Rosnąca częstość występowania chorób przewlekłych,-w tym cukrzycy, chorób układu krążenia i nowotworów,-tworzy zapotrzebowanie na technologie diagnostyczne i lecznicze. Rozwój infrastruktury opieki zdrowotnej na rynkach wschodzących otwiera nowe możliwości. Postęp technologiczny umożliwia wykorzystanie nowych możliwości urządzeń i zastosowań.
Przejście w stronę modeli opieki-opartych na wartości kładzie nacisk na poprawę wyników i redukcję kosztów, faworyzując urządzenia umożliwiające wcześniejszą diagnozę, mniej inwazyjne procedury i opiekę-w domu. Zdalne monitorowanie i integracja telezdrowia znacznie się rozwinęły podczas pandemii Covid-19 i nadal rosną, w miarę jak systemy opieki zdrowotnej wykorzystują modele opieki rozproszonej.
Wyzwania i wskazówki
Innowacje w zakresie wyrobów medycznych stoją w obliczu kilku ciągłych wyzwań.
Zagrożenia cyberbezpieczeństwa rosną wraz ze wzrostem łączności urządzeń. Urządzenia połączone w sieć stwarzają potencjalne luki w zabezpieczeniach wymagające solidnych środków bezpieczeństwa chroniących dane pacjentów i funkcjonalność urządzenia. Agencje regulacyjne coraz częściej sprawdzają funkcje cyberbezpieczeństwa podczas procesów zatwierdzania.
Odporność łańcucha dostaw okazała się kluczowym problemem podczas pandemii, ujawniając słabe punkty w globalnej produkcji i dystrybucji urządzeń. Firmy skupiają się obecnie na dywersyfikacji dostawców i regionalizacji produkcji, aby zmniejszyć ryzyko zakłóceń.
Interoperacyjność pozostaje wyzwaniem, ponieważ rozprzestrzenianie się urządzeń tworzy silosy danych. Systemy opieki zdrowotnej potrzebują urządzeń, które płynnie się komunikują, udostępniając dane pomiędzy platformami i dostawcami. Trwa rozwój standardów w celu usunięcia barier integracyjnych.
Harmonizacja przepisów mogłaby przyspieszyć dostępność urządzeń na całym świecie. Chociaż współpraca międzynarodowa zacieśniła się dzięki działaniom takim jak Międzynarodowe Forum Organów Regulacyjnych ds. Wyrobów Medycznych, różnice w wymaganiach regionalnych w dalszym ciągu utrudniają wprowadzanie urządzeń na wiele-rynków.
Względy zrównoważonego rozwoju w coraz większym stopniu wpływają na konstrukcję urządzenia. Urządzenia-jednorazowego użytku generują znaczne ilości odpadów medycznych, co zwiększa zainteresowanie alternatywami wielokrotnego użytku, materiałami nadającymi się do recyklingu oraz projektowaniem-z myślą o-praktykach zrównoważonego rozwoju, które minimalizują wpływ na środowisko.
Często zadawane pytania
Co odróżnia wyrób medyczny od leku?
Wyroby medyczne osiągają swój pierwotny cel za pomocą środków fizycznych, mechanicznych lub elektronicznych, a nie działania chemicznego. Leki działają poprzez mechanizmy farmakologiczne, metaboliczne lub immunologiczne. Urządzenie może dostarczać lek, ale samo urządzenie działa mechanicznie, podczas gdy lek działa chemicznie.
Czy wszystkie wyroby medyczne wymagają zgody FDA?
Nie wszystkie urządzenia wymagają tego samego poziomu zatwierdzenia. Wiele urządzeń klasy I jest zwolnionych z obowiązku powiadamiania przed wprowadzeniem na rynek. Urządzenia klasy II zazwyczaj wymagają zezwolenia 510(k), co oznacza znaczną równoważność z istniejącymi urządzeniami. Wyroby klasy III wymagają zatwierdzenia przed wprowadzeniem na rynek wraz z danymi klinicznymi. Konkretne wymagania zależą od klasyfikacji i przeznaczenia.
Czy oprogramowanie można uznać za wyrób medyczny?
Tak, oprogramowanie przeznaczone do celów medycznych kwalifikuje się jako wyrób medyczny nawet bez fizycznego sprzętu. Oprogramowanie jako urządzenie medyczne (SaMD) obejmuje algorytmy diagnostyczne, systemy wspomagania decyzji klinicznych i aplikacje do planowania leczenia. Agencje regulacyjne na całym świecie ustanowiły ramy dotyczące konkretnie wyrobów medycznych-opartych na oprogramowaniu.
Jak długo trwa zatwierdzenie wyrobu medycznego?
Terminy zatwierdzania różnią się znacznie w zależności od klasyfikacji urządzenia i ścieżki regulacyjnej.. 510(k) Zgoda trwa zwykle 3-12 miesięcy. Zatwierdzenie przed wprowadzeniem na rynek urządzeń klasy III często wymaga 1-3 lat lub dłużej, zwłaszcza gdy konieczne są badania kliniczne. Klasyfikacja de novo nowych wyrobów o niskim i umiarkowanym ryzyku trwa średnio 6–12 miesięcy.
Źródła danych
Światowa Organizacja Zdrowia - Definicja i klasyfikacja wyrobów medycznych (2020)
Amerykańska Agencja ds. Żywności i Leków - Przegląd i system klasyfikacji wyrobów medycznych
DataM Intelligence - Analiza rynku wyrobów medycznych w USA (2024)
Komisja Europejska - Rozporządzenie w sprawie wyrobów medycznych (UE) 2017/745
Projektowanie i outsourcing medyczny - Raport na temat innowacyjnych wyrobów medycznych (2024)
ScienceDirect - Formowanie wtryskowe metali w zastosowaniach medycznych (2020)














